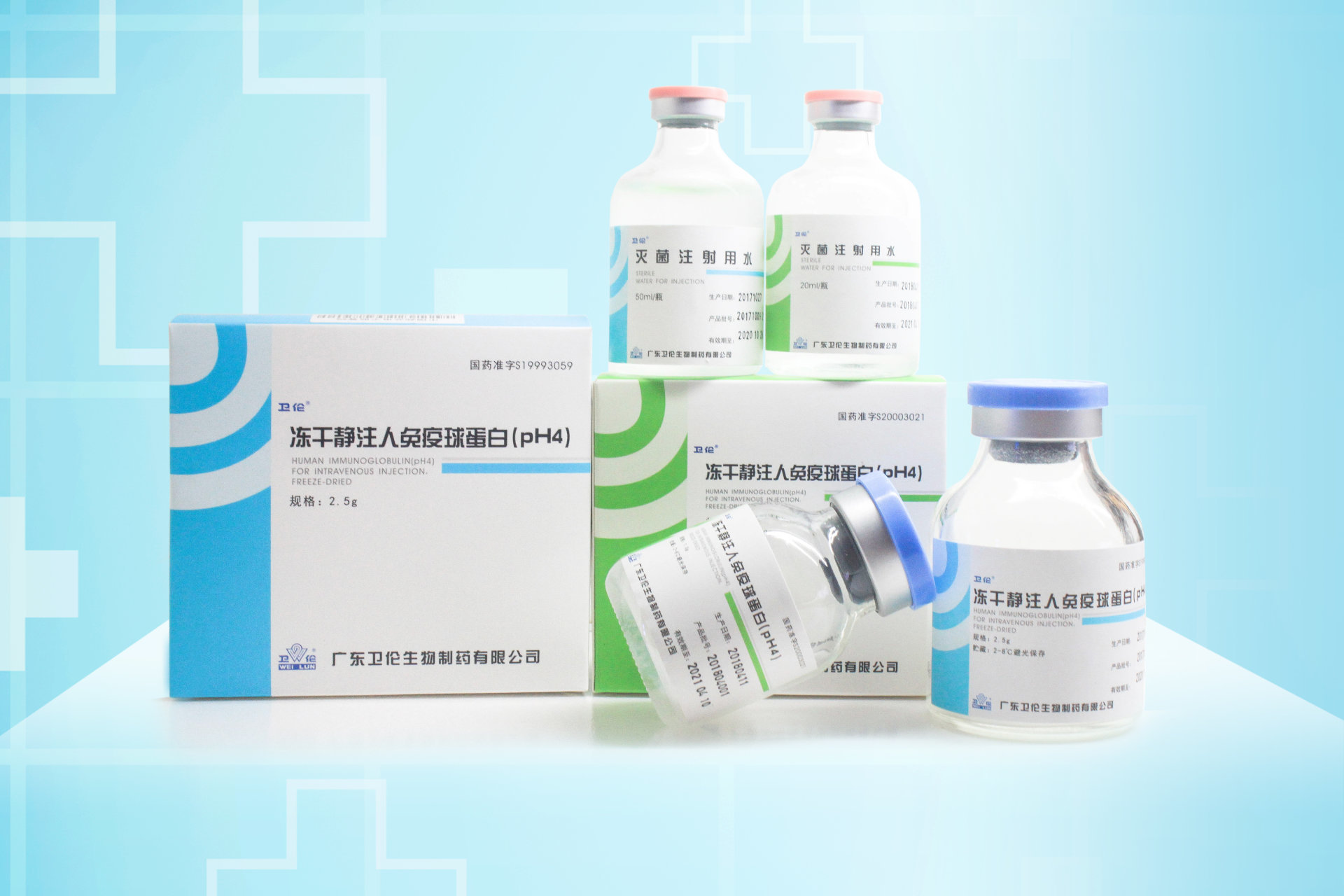
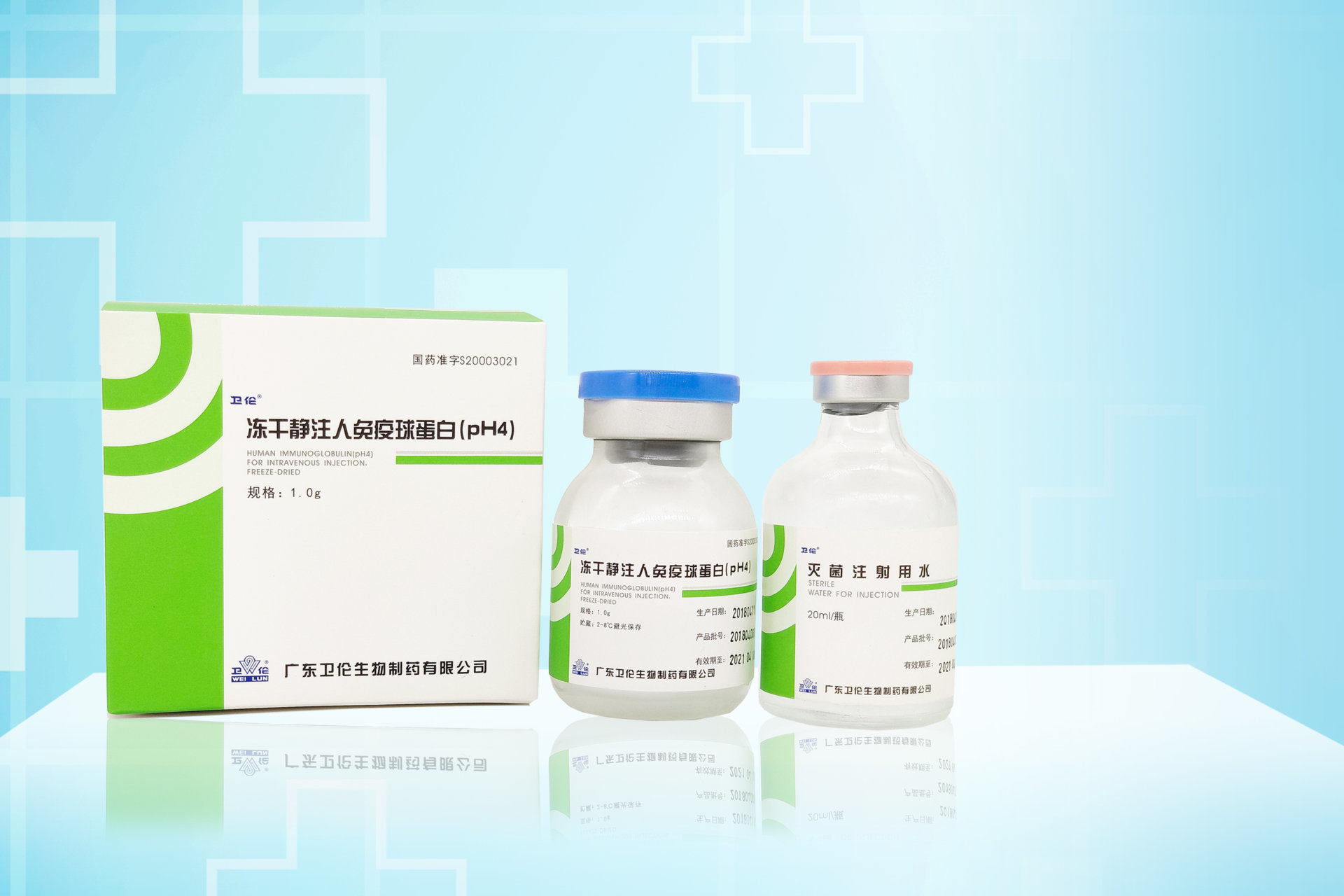
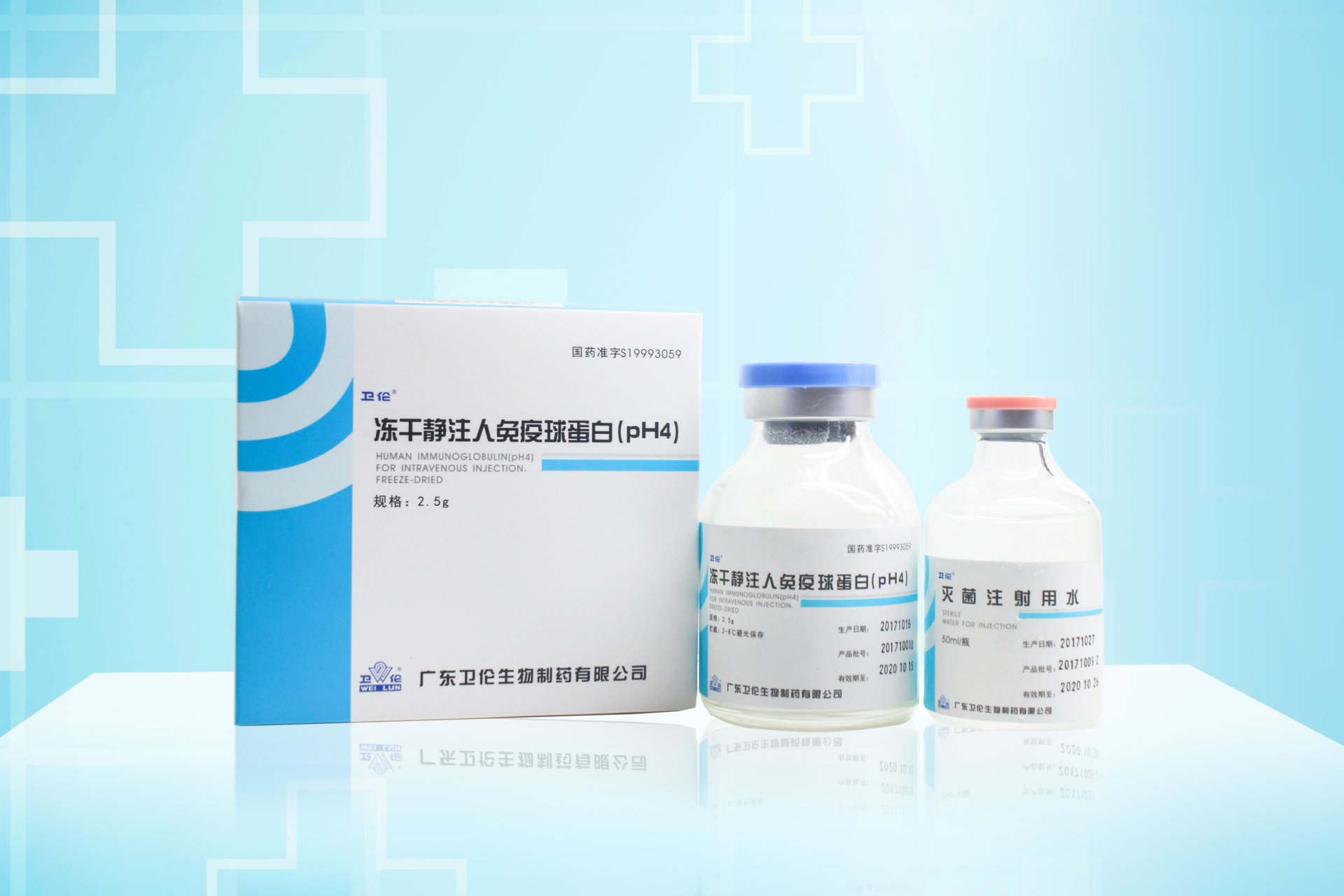
冻干静注人免疫球蛋白(pH4)
1.原发性免疫球蛋白缺乏症,如X联锁低免疫球蛋白血症,常见变异性免疫缺陷病,免疫球蛋白G亚型缺陷病等;
2.继发性免疫球蛋白缺陷病,如重症感染,新生儿败血症等;
3.自身免疫性疾病,如原发性血小板减少性紫癜,川崎病。
产品规格:2.5g、1.0g
关键词:
所属分类:
产品描述
冻干静注人免疫球蛋白(pH4)说明书
请仔细阅读说明书并在医师指导下使用
警示语:因原料来自人血,虽然对原料血浆进行了相关病原体的筛查,并在生产工艺中加入了去除和
灭活病毒的措施,但理论上仍存在传播某些已知和未知病原体的潜在风险,临床使用时应权衡利弊。
 [药品名称]
[药品名称]
通用名称:冻干静注人免疫球蛋白(pH4)
英文名称:Human Immunoglobulin(pH4) for Intravenous Injection,Freeze-dried
汉语拼音:Donggan Jingzhu Ren Mianyiqiudanbai(pH4)
 [成份]
[成份]
本品主要成份为人免疫球蛋白,系由健康人血浆,经低温乙醇蛋白分离法分离纯化,去除抗补体活性并经病毒灭活处理、冻干制成。含适宜稳定剂,不含防腐剂和抗生素。
 [性状]
[性状]
本品为白色疏松体,无融化迹象。复溶后为无色澄清液体,可带轻微乳光,不应出现浑浊。
 [适应症]
[适应症]
1.原发性免疫球蛋白缺乏症,如X联锁低免疫球蛋白血症,常见变异性免疫缺陷病,免疫球蛋白G亚型缺陷病等。
2.继发性免疫球蛋白缺陷病,如重症感染,新生儿败血症等。
3.自身免疫性疾病,如原发性血小板减少性紫癜,川崎病。
 [规格]
[规格]
2.5g、1.0g。
 [用法用量]
[用法用量]
用法:用灭菌注射用水将制品溶解至规定容积(规格为1.0g的溶解至20ml,规格为2.5g的溶解至50ml),静脉滴注或用5%葡萄糖溶液稀释1~2倍作静脉滴注,开始滴注速度为1.0ml/分(约20滴/分)持续15分钟后若无不良反应,可逐渐加快速度,最快滴注速度不得超过3.0ml/分(约60滴/分)。
用量:遵医嘱。推荐剂量:
1.原发性免疫球蛋白缺乏或低下症,首次剂量:400mg/kg体重;维持剂量:200~400mg/kg体重,给药间隔时间视病人血清IgG水平和病情而定,一般每月一次。
2.原发性血小板减少性紫癜:每日400 mg/kg体重,连续5日,维持剂量每次400mg/kg体重,间隔时间视血小板计数和病情而定,一般每周一次。
3.重症感染:每日200~300 mg/kg体重,连续2~3日。
4.川崎病:发病10日内应用,儿童治疗剂量2.0 g/kg体重,一次输注。
 [不良反应]
[不良反应]
一般无不良反应,极个别病人在输注时出现一过性头痛、心慌、恶心等不良反应,可能与输注速度过快或个体差异有关。上述反应大多轻微且常发生在输液开始一小时内,因此建议在输注的全过程定期观察病人的一般情况和生命特征,必要时减慢或暂停输注,一般无需特殊处理即可自行恢复。个别病人可在输注结束后发生上述反应,一般在24小时内均可自行恢复。
1.国外临床试验
同类的国外上市产品在超过5%的临床试验受试者中观察到以下常见不良反应:头痛、寒战、发热、疼痛、乏力、背痛、恶心、呕吐、腹痛、腹泻、输液部位反应、皮疹、瘙痒、荨麻疹、高血压、低血压、心动过速等。
2.国内上市后监测
本品及同类的国内上市产品监测到如下不良反应/事件,由于这些不良反应/事件是在无法确定总数的人群中自发报告的,因此不能准确估算其发生率:
(1)全身性损害:畏寒、高热、胸痛、不适、苍白、乏力、眶周水肿、水肿、全身酸痛等
(2)皮肤及其附件损害:斑丘疹、红斑性皮疹、局限性皮肤反应、表皮松解、多发性红斑、皮炎(如大疱性皮炎)、出汗增加等。
(3)免疫功能紊乱和感染:过敏反应、过敏样反应、输液反应、过敏性休克等。
(4)心血管系统损害:紫绀、心悸、高血压、心律失常等。
(5)神经系统损害:头晕、昏迷、意识丧失、震颤、肌肉不自主收缩、感觉减退等。
(6)呼吸系统损害:呼吸困难、呼吸急促、呼吸暂停、喘息、喉头水肿、呼吸功能不全、输血相关急性肺损伤、低氧血症等。
(7)血管损害和出凝血障碍:潮红、静脉炎等。
(8)精神障碍:激越、精神障碍、嗜睡等。
(9)代谢和营养障碍:高血糖。
(10)血液系统损害:白细胞减少、中性粒细胞减少、粒细胞缺乏等。
3.国外上市后监测
同类的国外上市产品还监测到如下不良反应/事件,由于这些不良反应/事件是在无法确定总数的人群中自发报告的,因此不能准确估算其发生率:
(1)皮肤及其附件损害:史蒂文斯-约翰逊综合征等。
(2)神经系统损害:癫痫发作、无菌性脑膜炎等。
(3)呼吸系统损害:急性呼吸窘迫综合征、肺水肿、支气管痉挛等。
(4)血管损害和出凝血障碍:血栓形成等。
(5)血液系统损害:血浆黏度增加、溶血反应等。
(6)泌尿系统损害:肾功能损害等。
 [禁忌]
[禁忌]
1.对人免疫球蛋白过敏或有其他严重过敏史者。
2.有抗IgA抗体的选择性IgA缺乏者。
 [注意事项]
[注意事项]
1.本品专供静脉输注用。
2.如需要,可以用5%葡萄糖溶液稀释本品,但糖尿病患者应慎用。
3.重溶后的药液呈现混浊、沉淀、异物或瓶子有裂纹、过期失效,不得使用。
4.本品开启后,应一次输注完毕,不得分次或给第二人输用。
5.有严重酸碱代谢紊乱的病人应慎用。
6.监测急性肾功能衰竭患者的肾功能,包括血尿素氮、血肌酐和尿量。对于肾功能不全或衰竭的患者,要以最小的速度输注。易感患者使用本品可能引起肾功能异常。使用含蔗糖的本品患者,更易引起肾功能异常和急性肾功能衰竭。
7.可能发生血栓性事件。监测有血栓形成事件已知危险因素的患者;对有高粘血症风险患者的血液粘度进行基线评估。对于有血栓形成风险的患者,要在最小剂量下缓慢输注。
8.可能发生无菌性脑膜炎综合征,特别是在高剂量或快速输注时。
9.可能发生溶血性贫血。监测溶血和溶血性贫血患者的临床体征和症状。
 [孕妇及哺乳期妇女用药]
[孕妇及哺乳期妇女用药]
对孕妇或可能怀孕妇女的用药应慎重,如有必要应用时,应在医师指导和严密观察下使用。
 [儿童用药]
[儿童用药]
未进行该项实验且无可靠参考文献。
 [老年用药]
[老年用药]
未进行该项试验研究,且无系统可靠的参考文献。在65岁以上的患者中,一般情况下,不超过推荐剂量,缓慢输注。
 [药物相互作用]
[药物相互作用]
本品应单独输注,不得与其他药物混合输用。
 [药物过量]
[药物过量]
未进行该项实验且无可靠参考文献。
 [药理毒理]
[药理毒理]
本品含有广谱抗病毒、细菌或其他病原体的IgG抗体,另外免疫球蛋白的独特型和独特型抗体形成复杂的免疫网络,所以具有免疫替代和免疫调节的双重治疗作用。经静脉输注后,能迅速提高受者血液中的IgG水平,增强机体的抗感染能力和免疫调节功能。
 [药代动力学]
[药代动力学]
未进行该项实验且无可靠参考文献。
 [贮藏]
[贮藏]
2-8℃避光保存。
 [包装]
[包装]
玻璃瓶,1瓶,配1瓶灭菌注射用水(50ml/瓶)。 2.5g
玻璃瓶,1瓶,配1瓶灭菌注射用水(20ml/瓶)。 1.0g
 [有效期]
[有效期]
36个月
 [执行标准]
[执行标准]
《中国药典》2015年版三部、YBS01642005
 [批准文号]
[批准文号]
国药准字S19993059 2.5g
国药准字S20003021 1.0g
 [药品上市许可持有人]
[药品上市许可持有人]
企业名称:广东卫伦生物制药有限公司
 [生产企业]
[生产企业]
广东卫伦生物制药有限公司
广东省汕头市濠江区珠浦工业区内
邮编:515071
电话:0754-87394218(公司总机)
传真:0754-87393327
相关内容
产品咨询

卫伦生物

卫伦人力资源